TEORI ATOM MODERN / TEORI ATOM MEKANIKA KUANTUM
Menurut Teori Atom Mekanika Kuantum (Teori Atom Modern), suatu kulit (tingkat energi) terdiri dari subkulit-subkulit (sub tingkat energi) dan suatu subkulit terdiri dari orbital.
- Subkulit s memiliki 1 orbital ⟶ maksimum ditempati 2 elektron
- Subkulit p memiliki 3 orbital ⟶ maksimum ditempati 6 elektron
- Subkulit d memiliki 5 orbital ⟶ maksimum ditempati 10 elektron
- Subkulit p memiliki 7 orbital ⟶ maksimum ditempati 14 elektron
Pengisian elektron ke dalam subkulit mengikuti prinsip Aufbau yakni elektron-elektron mengisi subkulit mulai dari yang berenergi rendah ke subkulit yang berenergi lebih tinggi, menurut bagan sebagai berikut :
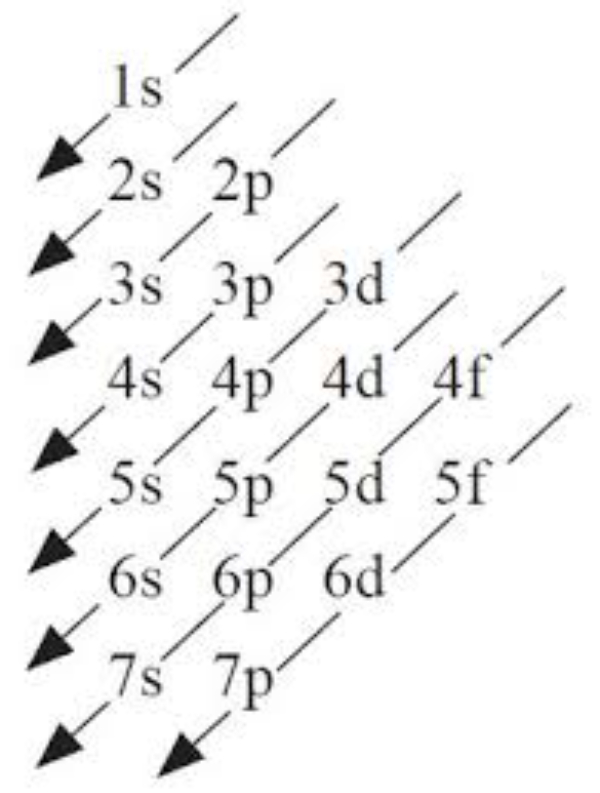
Urutan pengisian elektron menurut prinsip Aufbau:
1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s ... dst
Untuk mempermudah menghafal urutan pengisian elektron mengikuti prinsip Aufbau, maka dapat dibuat jembatan keledainya sebagai berikut:
saya suka pisang suka pisan suka dengan pisang suka dengan pisang suka feeling donat pisang suka feeling donat pisang sekali
Huruf depan dari setiap kata merepresentasikan subkulit s, p, d dan f.
Untuk 24X konfigurasi elektron menurut prinsip Aufbau adalah 1s2 2s2 2p6 3s2 3p6 4s2 3d4.
Namun, pada pengisian elektron, subkulit d cenderung penuh (berisi 10 elektron) atau setengah penuh (berisi 5 elektron), sehingga atom dengan struktur ns2 (n-1)d4 akan berubah menjadi ns1 (n-1)d5.
Jadi konfigurasi elektron untuk 24X adalah 1s2 2s2 2p6 3s2 3p6 4s1 3d5.