Prinsip Aufbau
Pengisian elektron ke dalam subkulit mengikuti prinsip Aufbau, yakni elektron-elektron mengisi subkulit mulai dari yang berenergi rendah ke subkulit yang berenergi lebih tinggi, menurut bagan sebagai berikut:
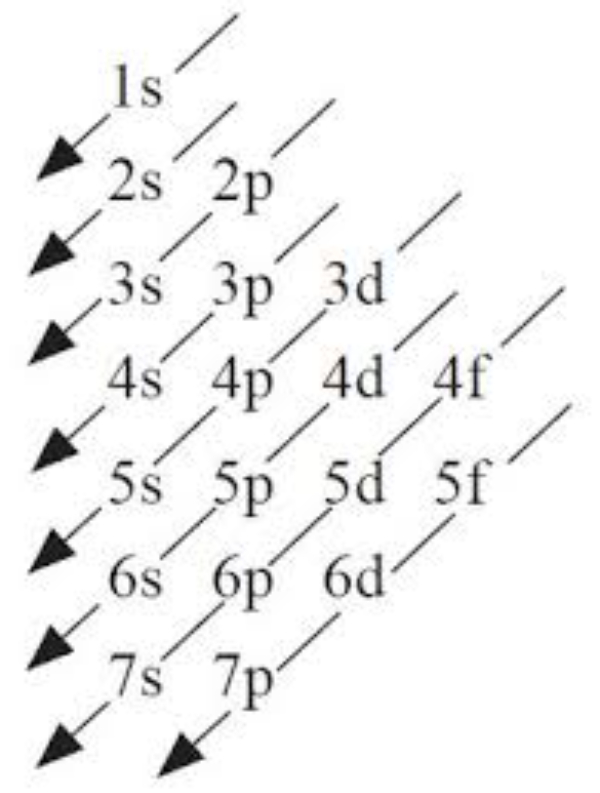
Urutan pengisian elektron menurut prinsip Aufbau:
1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s dst
Untuk mempermudah menghafal urutan pengisian elektron mengikuti prinsip Aufbau maka dapat dibuat jembatan keledainya sebagai berikut :
saya suka pisang suka pisang suka dengan pisang suka dengan pisang suka feeling donat pisang suka feeling donat pisang sekali
Huruf depan dari setiap kata merepresentasikan subkulit s, p, d dan f.
Aturan Hund
Pada tahun 1927, Friedrich Hund menyatakan aturan untuk menggambarkan arah rotasi elektron. Aturan ini dikenal sebagai aturan Hund yang berbunyi:
"Elektron-elektron yang berada di suatu orbital akan menempati orbital yang kosong dengan arah rotasi sejajar. Setelah itu, elektron-elektron lainnya menempati orbital tersebut dengan arah rotasi yang berlawanan".
Larangan Pauli
Prinsip larangan Pauli berkaitan dengan bilangan kuantum spin. Menurut Wolfgang Pauli, tidak ada elektron di dalam atom yang mempunyai keempat bilangan kuantum yang sama. Oleh karena itu, dua elektron dalam 1 orbital harus mempunyai spin yang berlawanan, yaitu +1/2 dan -1/2.
Jadi, pernyataan dua elektron dalam 1 orbital harus mempunyai spin yang berlawanan sesuai dengan pernyataan larangan Pauli.
*Adapun azas Heisenberg dan hipotesis de Broglie merupakan penemuan pada teori atom modern / mekanika kuantum.