TEORI ATOM MODERN / TEORI ATOM MEKANIKA KUANTUM
Menurut Teori Atom Mekanika Kuantum (Teori Atom Modern), suatu kulit (tingkat energi) terdiri dari subkulit-subkulit (sub tingkat energi) dan suatu subkulit terdiri dari orbital.
- Subkulit s memiliki 1 orbital ⟶ maksimum ditempati 2 elektron
- Subkulit p memiliki 3 orbital ⟶ maksimum ditempati 6 elektron
- Subkulit d memiliki 5 orbital ⟶ maksimum ditempati 10 elektron
- Subkulit f memiliki 7 orbital ⟶ maksimum ditempati 14 elektron
Pengisian elektron ke dalam subkulit mengikuti prinsip Aufbau, yakni elektron-elektron mengisi subkulit mulai dari yang berenergi rendah ke subkulit yang berenergi lebih tinggi, menurut bagan sebagai berikut:
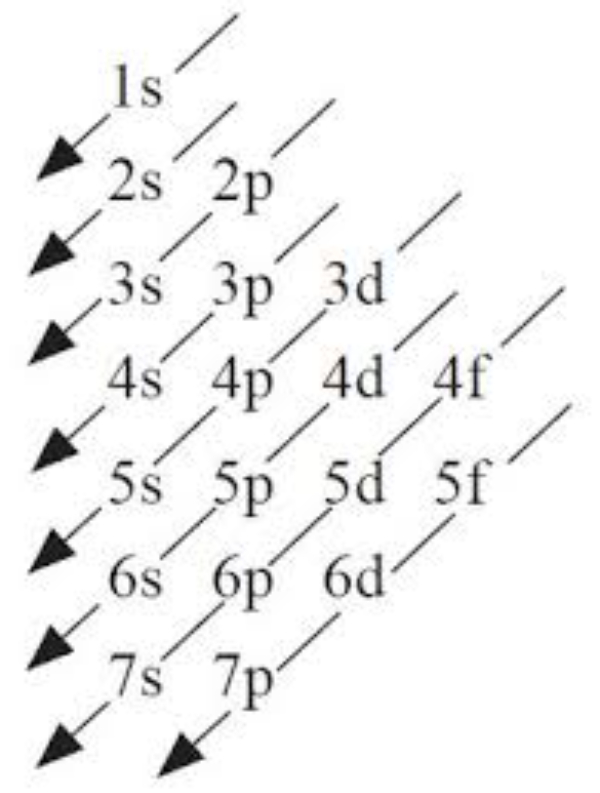
Urutan pengisian elektron menurut prinsip Aufbau:
1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s dst
Untuk mempermudah menghafal urutan pengisian elektron mengikuti prinsip Aufbau maka dapat dibuat jembatan keledainya sebagai berikut :
saya suka pisang suka pisang suka dengan pisang suka dengan pisang suka feeling donat pisang suka feeling donat pisang sekali
Huruf depan dari setiap kata merepresentasikan subkulit s, p, d dan f.
Aturan Hund
Pada tahun 1927, Friedrich Hund menyatakan aturan untuk menggambarkan arah rotasi elektron. Aturan ini dikenal sebagai aturan Hund yang berbunyi :
"Elektron-elektron yang berada di suatu orbital akan menempati orbital yang kosong dengan arah rotasi sejajar. Setelah itu, elektron-elektron lainnya menempati orbital tersebut dengan arah rotasi yang berlawanan".
Konfigurasi atom Fe = [Ar] 4s2 3d6 ⟶ elektron pada konfigurasi Ar dan orbital 4s2 terisi penuh sehingga semuanya berpasangan. Adapun pengisian elektron dari orbital 3d6 adalah
 ⟶ Berdasarkan pengisian elektron menurut aturan Hund, terdapat 4 elektron yang tidak berpasangan.
⟶ Berdasarkan pengisian elektron menurut aturan Hund, terdapat 4 elektron yang tidak berpasangan.
Jadi, dalam atom Fe dengan nomor atom 26, terdapat elektron yang tidak berpasangan sebanyak 4 elektron.