Konfigurasi elektron:
- 6C : 2 4
- 1H : 1
- 17Cl : 2 8 7
Elektron valensi atom pusat (C) = 4 elektron
Elektron yang dibutuhkan untuk berikatan dari 1 atom H = 1 elektron
Elektron yang dibutuhkan untuk berikatan dari 3 atom Cl (masing-masing 1) = 3 elektron
Jumlah elektron di sekitar atom pusat adalah 4 + 1 + 3 = 8 elektron atau 4 pasang.
Pasangan elektron ikatan (PEI) = 1 + 3 = 4 pasang. --> berikatan dengan 1 atom H dan 3 atom Cl
Pasangan elektron bebas (PEB) = 4 − 4 = 0 pasang.
Bentuk kerangka dasarnya AX4 dan bentuk molekul dari CHCl3 adalah bentuk tetrahedral.
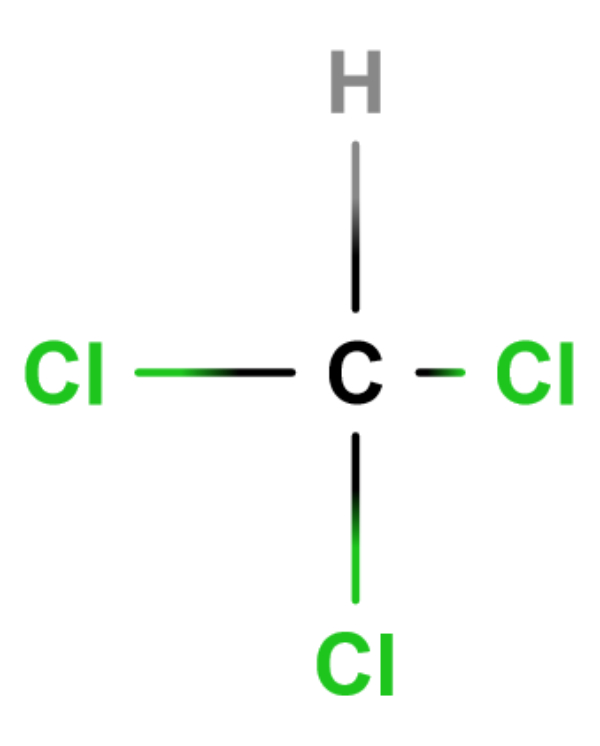
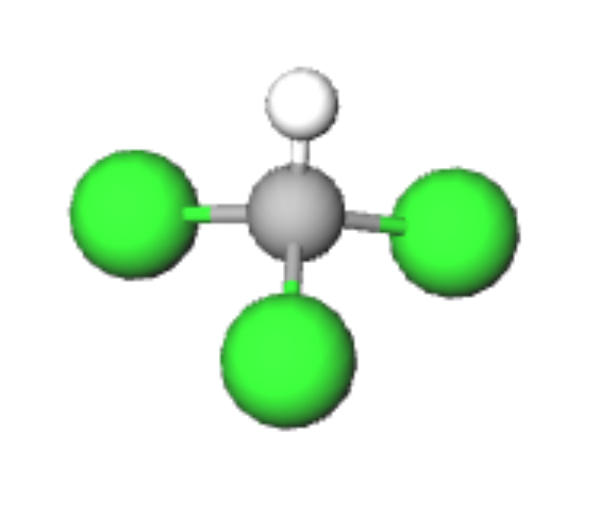
Konfigurasi elektron
- 54Xe : 2 8 18 18 8
- 9F : 2 7
Elektron valensi atom pusat (Xe) = 8 elektron
Elektron yang dibutuhkan untuk berikatan dari 2 atom F (masing-masing 1) = 2 elektron
Jumlah elektron di sekitar atom pusat = 8 + 2 = 10 elektron atau 5 pasang.
Pasangan elektron ikatan (PEI) = 2 pasang. --> berikatan dengan 2 atom F
Pasangan elektron bebas (PEB) = 5 − 2 = 3 pasang.
Bentuk kerangka dasarnya AX2E3 sehingga bentuk molekul dari XeF2 adalah linear.
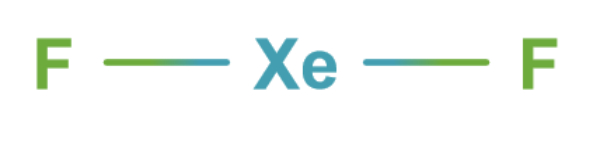
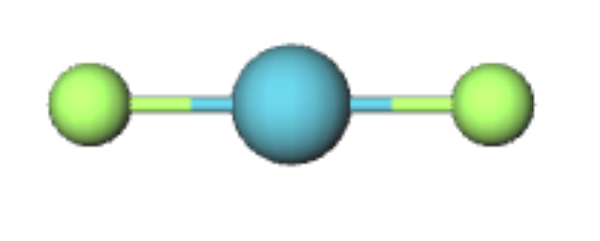
Konfigurasi elektron:
4Be : 2 2
17Cl : 2 8 7
Muatan BeCl2 = 0
Elektron valensi atom pusat (Be) = 2 elektron
Elektron yang dibutuhkan untuk berikatan dari 2 atom Cl (masing-masing 1) = 2 elektron
Jumlah elektron di sekitar atom pusat = 2 + 2 = 4 elektron atau 2 pasang.
Pasangan elektron ikatan (PEI) = 2 pasang. --> berikatan dengan 2 atom Cl
Pasangan elektron bebas (PEB) = 2 − 2 = 0 pasang.
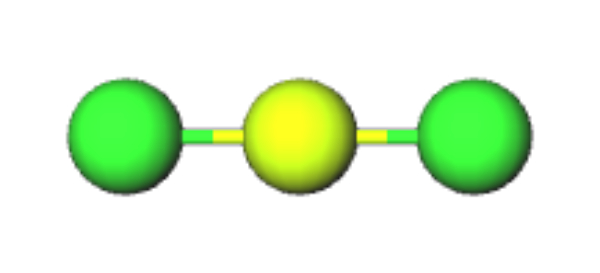
Bentuk kerangka dasarnya AX2 sehingga bentuk molekul dari BeCl2 adalah linear.

Konfigurasi elektron:
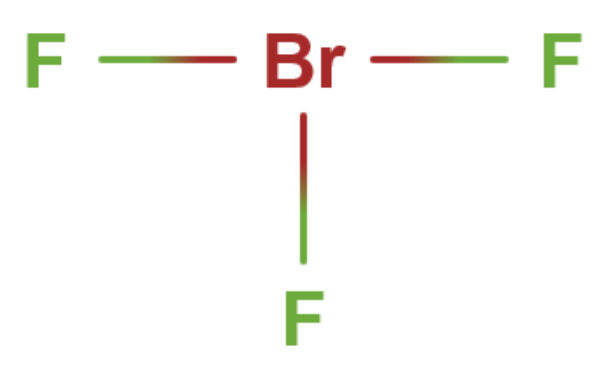
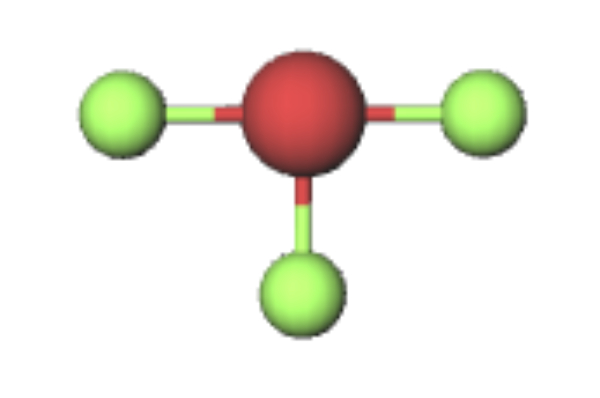
Elektron valensi atom pusat (Br) = 7 elektron
Elektron yang dibutuhkan untuk berikatan dari 3 atom F (masing-masing 1) = 3 elektron
Jumlah elektron di sekitar atom pusat = 7 + 3 = 10 elektron atau 5 pasang.
Pasangan elektron ikatan (PEI) = 3 pasang. --> berikatan dengan 3 atom F
Pasangan elektron bebas (PEB) = 5 − 3 = 2 pasang.
Bentuk kerangka dasarnya AX3E2 sehingga bentuk molekul dari BrF3 adalah bentuk T.
Konfigurasi elektron:
- 53I : 2 8 18 18 7
- 9F : 2 7
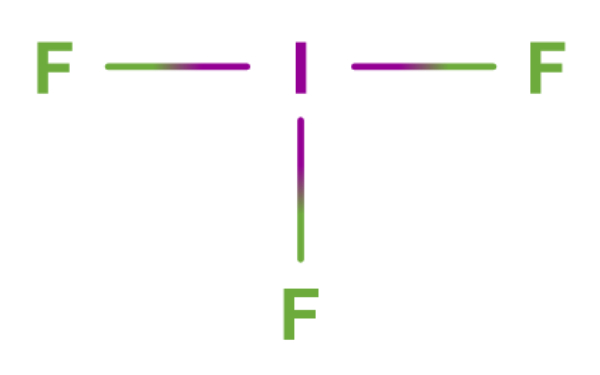
Elektron valensi atom pusat (I) = 7 elektron
Elektron yang dibutuhkan untuk berikatan dari 3 atom F (masing-masing 1) = 3 elektron
Jumlah elektron di sekitar atom pusat = 7 + 3 = 10 elektron atau 5 pasang.
Pasangan elektron ikatan (PEI) = 3 pasang. --> berikatan dengan 3 atom F
Pasangan elektron bebas (PEB) = 5 − 3 = 2 pasang.
Bentuk kerangka dasarnya AX3E2 sehingga bentuk molekul dari IF3 adalah bentuk T.
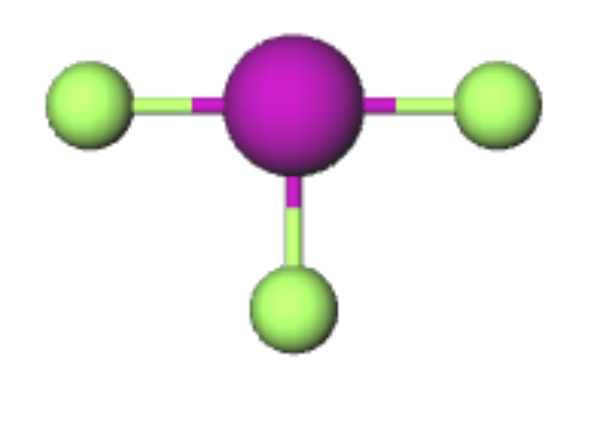
Maka, senyawa yang memiliki bentuk molekul tetrahedral adalah CHCl3.