Grafit tersusun dari atom karbon (C). Karbon memiliki nomor atom 6, berarti jumlah elektronnya adalah 6.
Konfigurasi atom karbon sebagai berikut
di kulit K terisi 2 elektron
di kulit L terisis 4 elektron
Dari konfigurasi di atas, kita dapat mengetahui bahwa atom C memiliki 4 elektron di kulit terluarnya (kulit L). Pada grafit, atom C berikatan dengan 3 atom C lainnya membentuk lapisan heksagonal (struktur datar yang berbentuk segi enam). Antar lapisan diikat oleh suatu gaya yang lemah yang disebut gaya Van der Waals.
Struktur grafit yang demikian menyebabkan grafit bersifat lunak dan lebih rapuh dibanding intan. Satu elektron yang tidak berikatan dapat berpindah-pindah dari satu atom C ke atom C lainnya (delokalisasi elektron) dalam satu lapisan yang sama. Oleh karena itu, grafit bersifat konduktor listrik atau dapat menghantarkan listrik.

Gambar intan (kiri) dan grafit (kanan)
sumber: intisari.grid.id
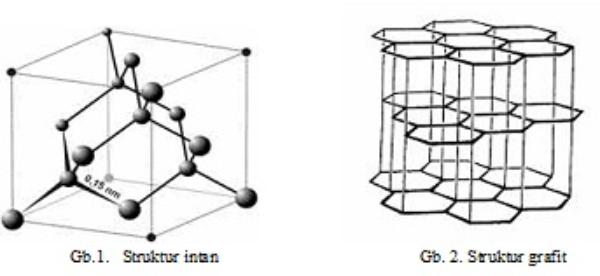
Struktur tetrahedral intan (kiri) dan struktur heksagonal grafit (kanan)
sumber: anisnaerni.wordpress.com
Jadi, sifat grafit ditunjuk oleh pernyataan nomor 1 dan 3.
*Pernyataan nomor 2 (bersifat sangat kuat dan keras) dan 4 (konduktor panas yang paling baik) adalah sifat dari intan.