Reaksi disproporsionasi adalah reaksi di mana satu unsur mengalami reaksi oksidasi sekaligus reaksi reduksi. Untuk menentukan hal itu, maka kita harus menentukan biloks masing-masing unsur kemudian melihat unsur manakah yang mengalami kenaikan atau penurunan biloks.
HOF
Karena HOF tidak memiliki muatan, maka nilai penjumlahan biloks unsur penyusunnya adalah 0.
Unsur H umumnya memiliki bilangan oksidasi +1. Unsur F termasuk unsur dalam golongan VIIA, sehingga memiliki biloks -1. Berdasarkan informasi tersebut, biloks O dapat ditentukan.
Biloks H + Biloks O + Biloks F = 0
+1 + Biloks O + (-1) = 0
Biloks O + 0 = 0
Biloks O = 0
H2O
Karena H2O tidak memiliki muatan, maka nilai penjumlahan biloks unsur penyusunnya adalah 0.
Unsur H umumnya memiliki bilangan oksidasi +1.
Biloks O + 2 × Biloks H = 0
Biloks O + 2(+1) = 0
Biloks O + 2 = 0
Biloks O = -2
OF2
Karena oksigen difluorida tidak memiliki muatan, maka nilai penjumlahan biloks unsur penyusunnya adalah 0.
Pada senyawa oksigen difluorida, terdapat pengecualian untuk biloks O di mana bukan sama dengan -2. Hal ini karena unsur F lebih elektronegatif daripada O sehingga biloks F yang bernilai negatif, yaitu -1 (golongan VIIA).
Biloks O + 2 × Biloks F = 0
Biloks O + 2(-1) = 0
Biloks O + (-2) = 0
Biloks O = +2
Setelah proses penentuan biloks di atas, perhatikan bagan berikut!
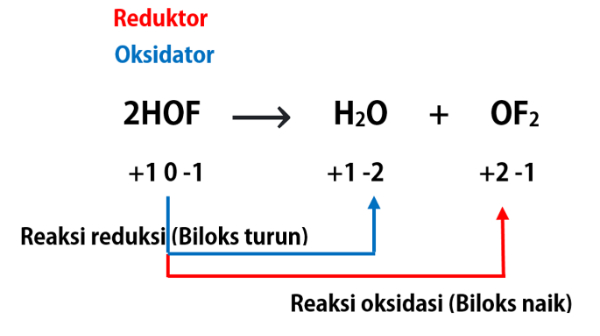
Berdasarkan reaksi di atas, yang mengalami disproporsionasi adalah O.