Kelarutan adalah jumlah maksimum zat yang dapat dilarutkan dalam sejumlah pelarut. Kelarutan dapat dinyatakan dalam dua jenis.
- Untuk zat yang mudah larut: dinyatakan dalam gram/100 gram air.
- Untuk zat yang sukar larut: dinyatakan dalam mol/L atau kemolaran.
Diketahui:
Ksp Mn(OH)2 = 4,9 × 10-14
[NaOH] = 0,1 M
V NaOH = 200 mL = 0,2 L
Ditanya: massa Mn(OH)2 dalam larutan NaOH?
Dijawab:
Mn(OH)2(s) ⇌ 2OH-(aq) + Mn2+(aq)
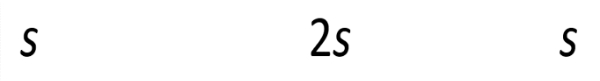
NaOH(aq) ⟶ Na+(aq) + OH-(aq)
[OH−]=[NaOH]=0,1 M
Proses pelarutan dalam natrium hidroksida 0,1 M.
[OH−]=(2s+0,1)≈0,1 M
[Mn2+]=s
Ksp=[OH−]2[Mn2+]
4,9×10−14=(0,1)2(s)
s=0,124,9×10−14
s=4,9×10−12
Maka kelarutan Mn(OH)2 dalam larutan NaOH sebesar 4,9 × 10-12 M.
[Mn(OH)2]=s=4,9×10−12 M
mol Mn(OH)2=[Mn(OH)2]×V pelarut
=4,9×10−12 M×0,2 L
=9,8×10−13 mol
massa Mn(OH)2=mol Mn(OH)2×Mr Mn(OH)2
=9,8×10−13 mol×89 g mol−1
=8,72×10−11 g
=8,72×10−8 mg
Maka massa mangan hidroksida yang dapat larut dalam 200 mL larutan NaOH 0,1 M yaitu sebesar 8,72 × 10-8 mg.