Rumus yang digunakan untuk menentukan konsentrasi ion H+ pada larutan penyangga asam adalah sebagai berikut.
[H+]=Ka×ga
Keterangan:
a = mol asam lemah (mol)
g = mol garam/basa konjugasi (mol)
Ka = tetapan ionisasi asam
Diketahui:
[HF]=0,02 M
[KOH]=0,01 M
VHF=30 mL
VKOH=30 mL
Ka=6,6×10−4
Ditanya: pH akhir?
Dijawab:
mol HF=[HF]×VHF
=0,02 M×30 mL
=0,6 mmol
mol KOH=[KOH]×VKOH
=0,01 M×30 mL
=0,3 mmol
Perhatikan bagan berikut!
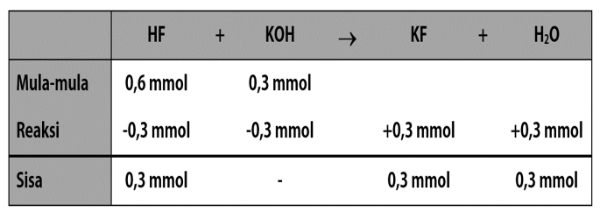
Karena yang tersisa adalah asam lemah (HF) dan garam/basa konjugasinya (KF), maka terbentuk larutan penyangga asam.
g=mol KF=0,3 mmol
a=mol HF=0,3 mmol
[H+]=Ka×ga
=6,6×10−4×0,30,3
=6,6×10−4
pH=−log[H+]
=−log(6,6×10−4)
=4−log6,6
=3,18
Maka pH larutan setelah reaksi selesai adalah 3,18.