Bank Soal Kimia SMA Pengaruh Ion Senama pada Kelarutan
Soal
Soal Populer Hari Ini
Berikut ini yang bukan merupakan kedudukan garis dan bidang dalam ruang adalah ....
Matematika
Level 12
Geometri
Dimensi Tiga (Geometri Ruang)
Kedudukan Titik, Garis, Bidang dalam Ruang
Ekspresi sama dengan ....
Matematika
Level 12
Trigonometri
Limit Fungsi Trigonometri
Nilai Limit Fungsi Trigonometri
Perhatikan tabel berikut!
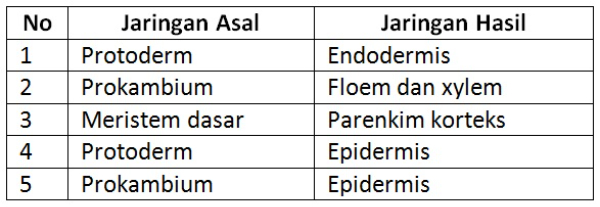
Pasangan jaringan asal dan jaringan hasil setelah terjadi perkembangan yang benar adalah nomor ....
Biologi
Level 12
Biologi
Pertumbuhan dan Perkembangan Makhluk Hidup
Pertumbuhan dan Perkembangan pada Tumbuhan
Which of the sentence is accepting a service?
Bahasa Inggris
Level 12
Bahasa Inggris
Services
Asking for and Giving Services
Complete the dialogue based on the situation.

You’re playing football in the park. You kick the ball a little bit too far and reaches a girl. She offers to give the ball back and you accept.
The girl: I’ll kick the ball back at the field!
You: _____.
Bahasa Inggris
Level 12
Bahasa Inggris
Services
Asking for and Giving Services
Bagaimana jasa pejuang Daan Mogot dalam revolusi kemerdekaan dan mempertahankan integrasi bangsa?
Sejarah Indonesia
Level 12
Upaya Bangsa Indonesia Menghadapi Ancaman Disintegrasi Bangsa
Tokoh Perjuangan Mempertahankan Integrasi Bangsa
Where should applicants write the address of the recipient?
Bahasa Inggris
Level 12
Bahasa Inggris
Application Letters
Application Letters
Persamaan garis normal pada kurva dengan di titik adalah ....
Matematika
Level 12
Trigonometri
Turunan Fungsi Trigonometri
Aplikasi Turunan Fungsi Trigonometri
Pada kondisi yang sama, di antara larutan berikut ini yang titik bekunya paling tinggi adalah ....
Kimia
Level 12
Sifat Koligatif Larutan
Sifat Koligatif Larutan Elektrolit
Andi mengambil sebuah bola dari kotak yang berisi 5 bolah merah dan 4 bola putih. Peluang bola yang diambil Andi berwarna merah adalah ....
Matematika
Level 12
Statistika
Peluang
Peluang Suatu Kejadian
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Berikut ini yang bukan merupakan kedudukan garis dan bidang dalam ruang adalah ....
Ekspresi sama dengan ....
Perhatikan tabel berikut!
Pasangan jaringan asal dan jaringan hasil setelah terjadi perkembangan yang benar adalah nomor ....
Which of the sentence is accepting a service?
Complete the dialogue based on the situation.

You’re playing football in the park. You kick the ball a little bit too far and reaches a girl. She offers to give the ball back and you accept.
The girl: I’ll kick the ball back at the field!
You: _____.
Bagaimana jasa pejuang Daan Mogot dalam revolusi kemerdekaan dan mempertahankan integrasi bangsa?
Where should applicants write the address of the recipient?
Persamaan garis normal pada kurva dengan di titik adalah ....
Pada kondisi yang sama, di antara larutan berikut ini yang titik bekunya paling tinggi adalah ....
Andi mengambil sebuah bola dari kotak yang berisi 5 bolah merah dan 4 bola putih. Peluang bola yang diambil Andi berwarna merah adalah ....