Bank Soal Kimia SMA Perhitungan Kimia dan Kadar Zat dalam Campuran
Soal
Soal Populer Hari Ini
Bilangan 73 ... 102
Matematika
Level 2
Bilangan
Mengenal Bilangan Cacah (0-999)
Membandingkan dan Mengurutkan Bilangan
Fizi pergi ke kantin.
Di kantin tersebut menjual berbagai macam minuman.
Berikut adalah daftar harga berbagai macam minuman yang dijual.

(Sumber Gambar: flaticon.com)
Fizi memiliki 1 lembar uang sepuluh ribuan.
Ia ingin menggunakan uangnya untuk membeli 2 jenis minuman tanpa mendapatkan uang kembalian.
Minuman yang dapat dibeli Fizi adalah ....
Matematika
Level 2
Bilangan
Nilai dan Kesetaraan Mata Uang
Kesetaraan Nilai Mata Uang
Perhatikan gambar kubus berikut!
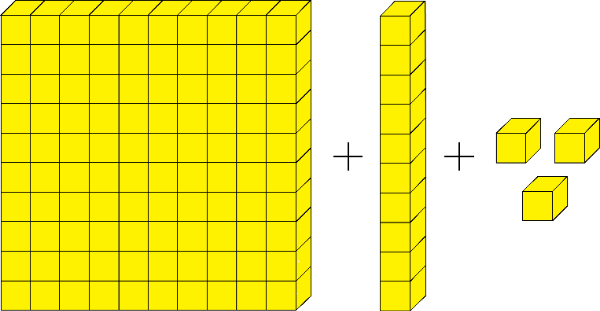
Dengan catatan:
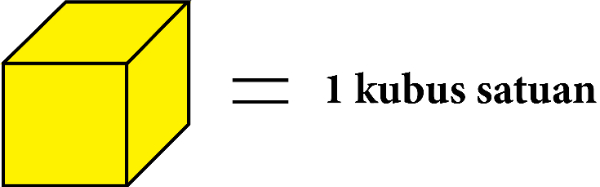
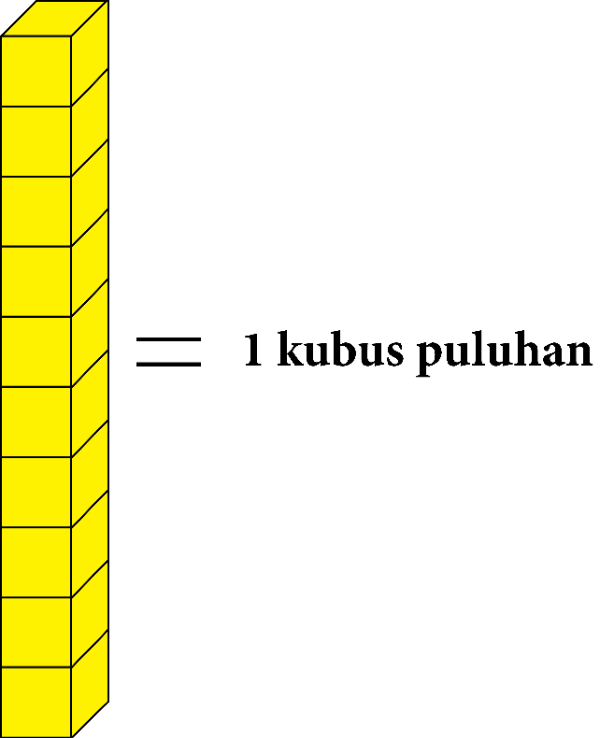
Kubus satuan yang berjumlah sepuluh digambarkan menjadi 1 kubus puluhan.
Dan kubus puluhan yang berjumlah sepuluh digambarkan menjadi kubus ratusan.
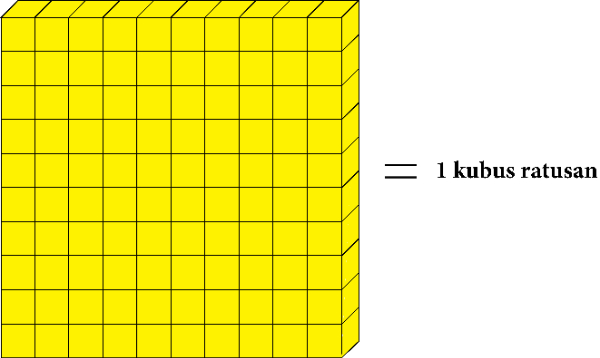
Banyaknya kubus pada gambar di atas ada ....
Matematika
Level 2
Bilangan
Mengenal Bilangan Cacah (0-999)
Mengenal Bilangan Sampai 999
24 4 = ....
Matematika
Level 2
Bilangan
Perkalian dan Pembagian Bilangan Cacah
Perkalian dan Pembagian Bilangan Cacah

(Sumber: freepik.com)
Perhatikan bangun ruang yang memiliki ciri-ciri sebagai berikut:
1. Memiliki 8 sisi,
2. Memiliki 2 sisi berbentuk segienam dan 6 sisi berbentuk persegi panjang,
3. Memiliki 12 titik sudut,
4. Memiliki 18 rusuk.
Bangun ruang yang memiliki ciri-ciri di atas ditunjukkan oleh bangun ruang yang berbentuk ....
Matematika
Level 2
Geometri
Bangun Ruang sederhana
Rusuk, Sisi, Ruas Garis
Perhatikan gambar berikut!!

(Sumber Gambar: freepik.com)
Banyaknya segi enam pada gambar di atas ada ... buah.
Matematika
Level 2
Geometri
Bangun Datar Sederhana
Ciri-Ciri Bangun Datar Sederhana
Bacalah teks percakapan berikut ini!
Mika: Boni, ayo, nanti sore kamu ikut bersepeda bersama aku dan Yoga.
Boni: Maaf, Mika. Aku tidak bisa ikut karena aku tidak punya sepeda.
Yoga: Kalau begitu, yuk, nanti sore kita bermain sepak bola di lapangan.
Boni: Maaf, Yoga. Aku tidak bisa ikut karena aku tidak punya sepatu sepak bola.
Mika: Baiklah. Ayo, nanti sore kita main di rumahku saja. Kebetulan aku punya mainan baru.
Yoga: Oke, Mika. Nanti sore aku akan datang ke rumahmu. Bagaimana denganmu, Boni?
Boni: Aku bisa, teman-teman. Nanti sore aku akan datang ke rumah Mika.
Ungkapan ajakan yang diucapkan Mika dalam teks percakapan di atas adalah sebagai berikut, kecuali ...
Bahasa Indonesia
Level 2
Menulis
Ungkapan (1)
Ungkapan Ajakan

Nilai tempat ... sama pada kedua bilangan di atas.
Matematika
Level 2
Bilangan
Mengenal Bilangan Cacah (0-999)
Menentukan Nilai Tempat Bilangan
Di taman terdapat beberapa kumbang seperti pada gambar.
Kumbang-kumbang tersebut ada yang terbang dan ada yang masih hinggap di dedaunan maupun bunga.

(Sumber: freepik.com)
Bilangan pecahan yang menyatakan jumlah kumbang yang terbang adalah ....
Matematika
Level 2
Bilangan
Konsep Pecahan
Konsep Pecahan
Perhatikan gambar berikut!


(Sumber Gambar: id.wikipedia.org)
Pecahan uang yang setara dengan uang pada gambar di atas adalah ....
Matematika
Level 2
Bilangan
Nilai dan Kesetaraan Mata Uang
Kesetaraan Nilai Mata Uang
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Bilangan 73 ... 102
Fizi pergi ke kantin.
Di kantin tersebut menjual berbagai macam minuman.
Berikut adalah daftar harga berbagai macam minuman yang dijual.
(Sumber Gambar: flaticon.com)
Fizi memiliki 1 lembar uang sepuluh ribuan.
Ia ingin menggunakan uangnya untuk membeli 2 jenis minuman tanpa mendapatkan uang kembalian.
Minuman yang dapat dibeli Fizi adalah ....
Perhatikan gambar kubus berikut!
Dengan catatan:
Kubus satuan yang berjumlah sepuluh digambarkan menjadi 1 kubus puluhan.
Dan kubus puluhan yang berjumlah sepuluh digambarkan menjadi kubus ratusan.

Banyaknya kubus pada gambar di atas ada ....
24 4 = ....
(Sumber: freepik.com)
Perhatikan bangun ruang yang memiliki ciri-ciri sebagai berikut:
1. Memiliki 8 sisi,
2. Memiliki 2 sisi berbentuk segienam dan 6 sisi berbentuk persegi panjang,
3. Memiliki 12 titik sudut,
4. Memiliki 18 rusuk.
Bangun ruang yang memiliki ciri-ciri di atas ditunjukkan oleh bangun ruang yang berbentuk ....
Perhatikan gambar berikut!!
(Sumber Gambar: freepik.com)
Banyaknya segi enam pada gambar di atas ada ... buah.
Bacalah teks percakapan berikut ini!
Mika: Boni, ayo, nanti sore kamu ikut bersepeda bersama aku dan Yoga.
Boni: Maaf, Mika. Aku tidak bisa ikut karena aku tidak punya sepeda.
Yoga: Kalau begitu, yuk, nanti sore kita bermain sepak bola di lapangan.
Boni: Maaf, Yoga. Aku tidak bisa ikut karena aku tidak punya sepatu sepak bola.
Mika: Baiklah. Ayo, nanti sore kita main di rumahku saja. Kebetulan aku punya mainan baru.
Yoga: Oke, Mika. Nanti sore aku akan datang ke rumahmu. Bagaimana denganmu, Boni?
Boni: Aku bisa, teman-teman. Nanti sore aku akan datang ke rumah Mika.
Ungkapan ajakan yang diucapkan Mika dalam teks percakapan di atas adalah sebagai berikut, kecuali ...
Nilai tempat ... sama pada kedua bilangan di atas.
Di taman terdapat beberapa kumbang seperti pada gambar.
Kumbang-kumbang tersebut ada yang terbang dan ada yang masih hinggap di dedaunan maupun bunga.
(Sumber: freepik.com)
Bilangan pecahan yang menyatakan jumlah kumbang yang terbang adalah ....
Perhatikan gambar berikut!
(Sumber Gambar: id.wikipedia.org)
Pecahan uang yang setara dengan uang pada gambar di atas adalah ....







