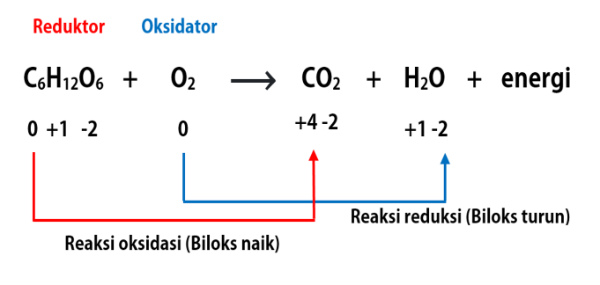
Karbon dioksida atau CO2
Karena karbon dioksida tidak memiliki muatan, maka nilai penjumlahan biloks unsur penyusunnya adalah 0. Unsur O termasuk unsur pada golongan VIA, sehingga memiliki bilangan oksidasi -2. Dari informasi tersebut, kita dapat menentukan biloks C.
Biloks C + 2 × Biloks O = 0
Biloks C + 2(-2) = 0
Biloks C + (-4) = 0
Biloks C = +4
Sehingga biloks C dan O pada karbon dioksida berturut-turut adalah +4 dan -2.
Air atau H2O
Karena air tidak memiliki muatan, maka nilai penjumlahan biloks unsur penyusunnya adalah 0. Unsur O termasuk unsur pada golongan VIA, sehingga memiliki bilangan oksidasi -2. Unsur H umumnya memiliki biloks +1.
Sehingga biloks H dan O pada air berturut-turut adalah +1 dan -2.
Glukosa atau C6H12O6
Karena C6H12O6 tidak memiliki muatan, maka nilai penjumlahan biloks unsur penyusunnya adalah 0. Unsur H umumnya memiliki biloks +1. Unsur O termasuk unsur pada golongan VIA, sehingga memiliki bilangan oksidasi -2. Dari informasi tersebut, kita dapat menentukan biloks C.
6 × Biloks C + 12 × Biloks H + 6 × Biloks O = 0
6 × Biloks C + 12(+1) + 6(-2) = 0
6 × Biloks C + 12 + (-12) = 0
6 × Biloks C + 0 = 0
Biloks C = 0
Sehingga biloks C, H, dan O pada karbon dioksida berturut-turut adalah 0, +1 dan -2.
Oksigen atau O2
Karena oksigen termasuk unsur bebas maka biloks O pada oksigen bernilai 0.
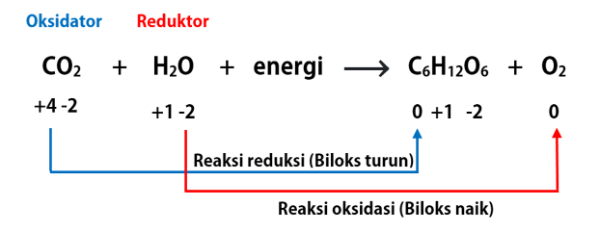
Berdasarkan penentuan biloks tiap unsur pada senyawa yang terdapat di reaksi:
- unsur yang mengalami kenaikan biloks adalah O pada H2O menjadi O2, yaitu dari -2 menjadi 0. Reaksi ini disebut reaksi oksidasi;
- unsur yang mengalami penurunan biloks terjadi pada unsur C pada senyawa karbon dioksida menjadi glukosa, yaitu dari +4 menjadi 0. Reaksi ini disebut reaksi reduksi.
Maka dapat disimpulkan unsur yang mengalami penurunan biloks adalah unsur C berasal dari senyawa CO2 (karbon dioksida) menjadi senyawa C6H12O6 (glukosa) dengan perubahan biloks dari +4 menjadi 0.