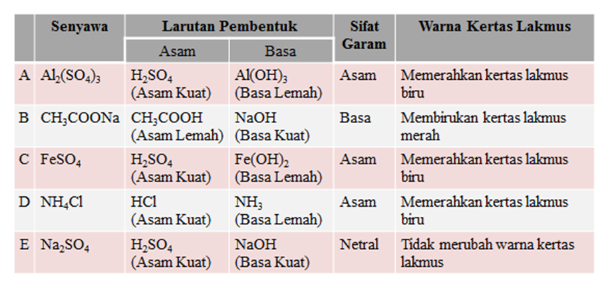
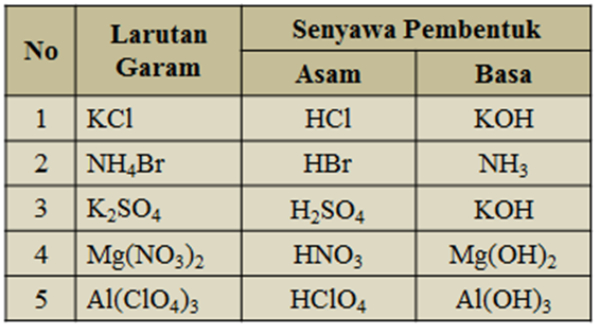
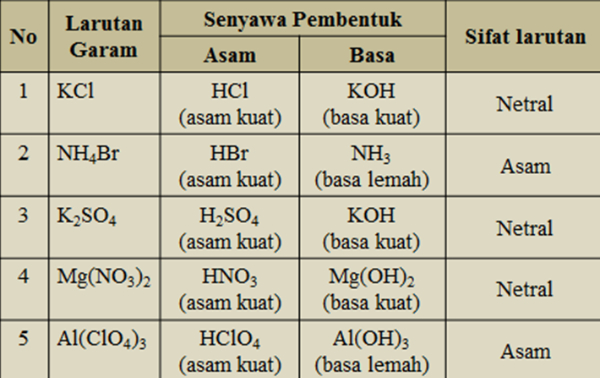
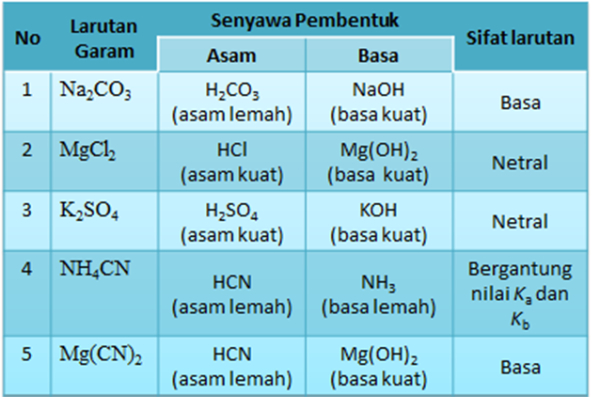
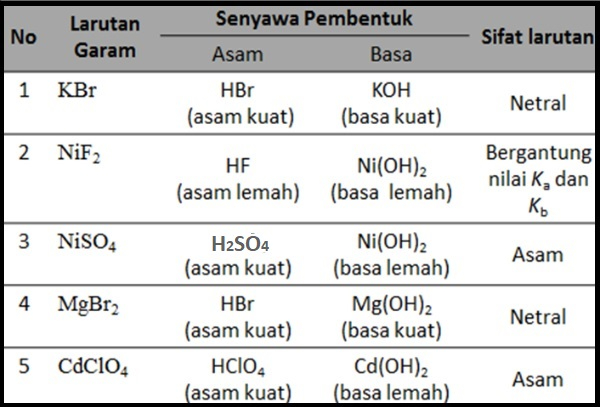
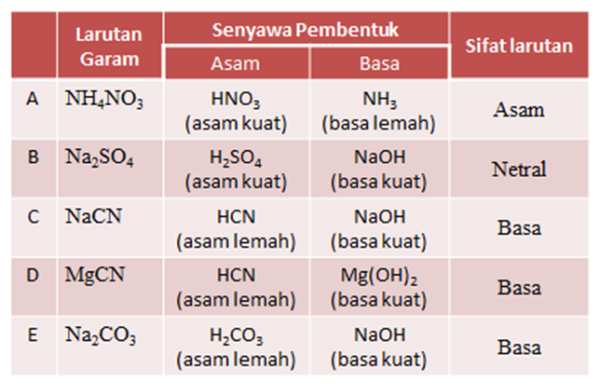
Garam yang bersifat netral yaitu garam yang tidak terhidrolisis, sehingga jumlah ion H+ dan ion OH- tetap. Oleh karena itu adanya garam tidak mempengaruhi pH air murni. Berikut penjelasannya:
ZnCl2 terionisasi dalam air menurut persamaan reaksi berikut:
ZnCl2(aq) ⟶ Zn2+(aq) + 2Cl-(aq)
Ion Zn2+ berasal dari basa lemah Zn(OH)2 sehingga dapat bereaksi dengan air. Persamaan reaksinya yaitu:
Zn2+(aq) + 2H2O(l) ⟶ Zn(OH)2(aq) + 2H+(aq)
Ion Cl- berasal dari asam kuat HCl, sehingga tidak dapat bereaksi dengan air.
Jadi, garam ZnCl2 terhidrolisis sebagian dan menghasilkan ion H+ sehingga larutan tersebut akan bersifat asam.
CH3COONa terionisasi dalam air menurut persamaan reaksi berikut:
CH3COONa(aq) ⟶ Na+(aq) + CH3COO-(aq)
Ion Na+ berasal dari basa kuat NaOH sehingga tidak dapat bereaksi dengan air.
Ion CH3COO- berasal dari asam lemah CH3COOH sehingga dapat bereaksi dengan air. Persamaan reaksinya yaitu:
CH3COO-(aq) + H2O(l) ⟶ CH3COOH(aq) + OH-(aq)
Jadi, garam CH3COONa merupakan garam yang terhidrolisis sebagian dan menghasilkan ion OH- sehingga larutan tersebut akan bersifat basa.
K3PO4 terionisasi dalam air menurut persamaan reaksi berikut:
K3PO4(aq) ⟶ 3K+(aq) + PO33-(aq)
Ion K+ berasal dari basa kuat KOH sehingga tidak dapat bereaksi dengan air.
Ion PO33- berasal dari asam lemah H3PO3, sehingga dapat bereaksi dengan air. Persamaan reaksinya yaitu:
PO33-(aq) + 3H2O(l) ⟶ H3PO3(aq) + 3OH-(aq)
Jadi, garam K3PO3 terhidrolisis sebagian dan menghasilkan ion OH- sehingga larutan tersebut akan bersifat basa.
Na2SO4 terionisasi dalam air menurut persamaan reaksi berikut:
Na2SO4(aq) ⟶ 2Na+(aq) + SO42-(aq)
Ion Na+ berasal dari basa kuat NaOH sehingga tidak dapat bereaksi dengan air.
Ion SO42- berasal dari asam kuat H2SO4, sehingga tidak dapat bereaksi dengan air.
Jadi, pada garam Na2SO4 merupakan garam yang tidak terhidrolisis, sehingga konsentrasi ion H+ sama dengan konsentrasi ion OH- dan larutan tersebut akan bersifat netral.
AgBr terionisasi dalam air menurut persamaan reaksi berikut:
AgBr(aq) ⟶ Ag+(aq) + Br-(aq)
Ion Ag+ berasal dari basa lemah AgOH sehingga dapat bereaksi dengan air. Persamaan reaksinya yaitu:
Ag+(aq) + H2O(l) ⟶ AgOH(aq) + H+(aq)
Ion Br- berasal dari asam kuat HBr, sehingga tidak dapat bereaksi dengan air.
Jadi, garam AgBr terhidrolisis sebagian dan menghasilkan ion H+ sehingga larutan tersebut akan bersifat asam.
Jadi, larutan garam yang bersifat netral adalah Na2SO4.