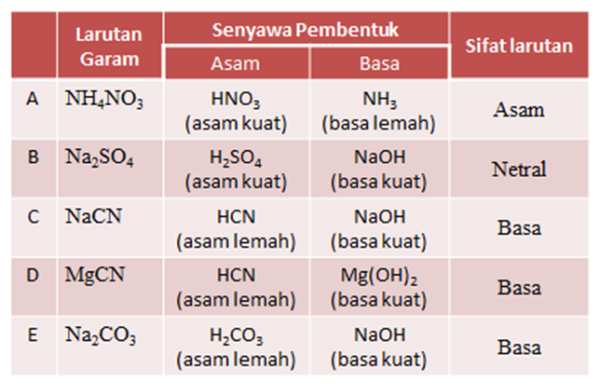
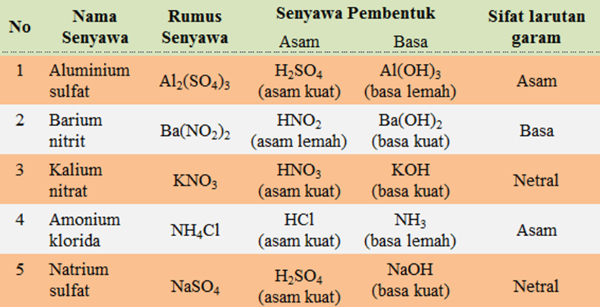
Garam NaCl adalah garam yang kationnya berasal dari basa kuat NaOH dan anionnya berasal dari asam kuat HCl, sehingga kedua ion tidak terhidrolisis dalam air dan garam bersifat netral. Garam yang tidak terhidrolisis memiliki jumlah ion H+ dan ion OH- tetap. Oleh karena itu, adanya garam tidak memengaruhi pH air murni. Berikut penjelasannya:
ZnBr2 terionisasi dalam air menurut persamaan reaksi berikut:
ZnBr2(aq) ⟶ Zn2+(aq) + 2Br-(aq)
Ion Zn2+ berasal dari basa lemah Zn(OH)2 sehingga dapat bereaksi dengan air. Persamaan reaksinya yaitu:
Zn2+(aq) + 2H2O(l) ⟶ Zn(OH)2(aq) + 2H+(aq)
Ion Br- berasal dari asam kuat HBr sehingga tidak dapat bereaksi dengan air.
Jadi, garam ZnBr2 merupakan garam yang terhidrolisis sebagian dan bersifat asam.
(HCOO)2Mg terionisasi dalam air menurut persamaan reaksi berikut:
(HCOO)2Mg(aq) ⟶ Mg2+(aq) + 2HCOO-(aq)
Ion Mg2+ berasal dari basa kuat Mg(OH)2 sehingga tidak dapat bereaksi dengan air.
Ion HCOO- berasal dari asam lemah HCOOH sehingga dapat bereaksi dengan air. Persamaan reaksinya yaitu:
HCOO-(aq) + H2O(l) ⟶ HCOOH(aq) + OH-(aq)
Jadi, garam (HCOO)2Mg merupakan garam yang terhidrolisis sebagian dan bersifat basa.
K3PO3 terionisasi dalam air menurut persamaan reaksi berikut:
K3PO3(aq) ⟶ 3K+(aq) + PO33-(aq)
Ion K+ berasal dari basa kuat KOH sehingga tidak dapat bereaksi dengan air.
Ion PO33- berasal dari asam lemah H3PO3 sehingga dapat bereaksi dengan air. Persamaan reaksinya yaitu:
PO33-(aq) + 3H2O(l) ⟶ H3PO3(aq) + 3OH-(aq)
Jadi, garam K3PO3 merupakan garam yang terhidrolisis sebagian dan bersifat basa.
BaSO4 terionisasi dalam air menurut persamaan reaksi berikut:
BaSO4(aq) ⟶ Ba2+(aq) + SO42-(aq)
Ion Ba2+ berasal dari basa kuat Ba(OH)2 sehingga tidak dapat bereaksi dengan air.
Ion SO42- berasal dari asam kuat H2SO4 sehingga tidak dapat bereaksi dengan air.
Jadi, garam BaSO4 merupakan garam yang tidak terhidrolisis dan bersifat netral.
AgCl terionisasi dalam air menurut persamaan reaksi berikut:
AgCl(aq) ⟶ Ag+(aq) + Cl-(aq)
Ion Ag+ berasal dari basa lemah AgOH sehingga dapat bereaksi dengan air. Persamaan reaksinya yaitu:
Ag+(aq) + H2O(l) ⟶ AgOH(aq) + H+(aq)
Ion Cl- berasal dari asam kuat HCl sehingga tidak dapat bereaksi dari air.
Jadi, garam AgCl merupakan garam yang terhidrolisis sebagian dan bersifat asam.
Jadi, larutan garam yang memiliki kesamaan sifat dengan garam NaCl adalah garam BaSO4.