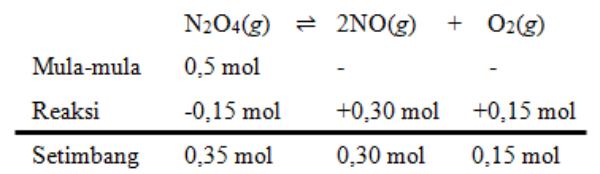Diketahui:
- V = 2 L
- n awal N2O4 = 0,5 mol
- α = 30%
Ditanyakan:
Kc?
Dijawab:
Tetapan Kesetimbangan ⟶ Pada suhu tertentu, hasil kali konsentrasi zat-zat produk yang dipangkatkan koefisien reaksinya, dibagi dengan hasil kali konsentrasi zat-zat reaktan yang dipangkatkan dengan koefisien reaksinya.
Secara umum untuk reaksi kesetimbangan berikut:
aA(g) + bB(g) ⇌ cC(g) + dD(g)
rumusan tetapan kesetimbangan berdasarkan konsentrasi (Kc) adalah
Kc=[A]a[B]b[C]c[D]d
Keterangan:
- [A] = konsentrasi kesetimbangan A
- [B] = konsentrasi kesetimbangan B
- [C] = konsentrasi kesetimbangan C
- [D] = konsentrasi kesetimbangan D
*Zat padat murni (s) dan zat cair murni (l) tidak disertakan dalam persamaan tetapan kesetimbangan berdasarkan konsentrasi.
Untuk reaksi:
N2O4(g) ⇌ 2NO(g) + O2(g)
Tetapan kesetimbangannya adalah
Kc=[N2O4][NO]2[O2]
- Tentukan mol pada saat reaksi (mol yang terdisosiasi)
α=mol mula−mulamol yang terdisosiasi×100%
mol yang terdisosiasi=100%α×mol mula-mula
mol yang terdisosiasi=100%30%×0,5 mol
mol yang terdisosiasi=0,15 mol
- Buat persamaan reaksi kesetimbangan dan tentukan mol mula-mula, mol reaksi, dan mol saat setimbang
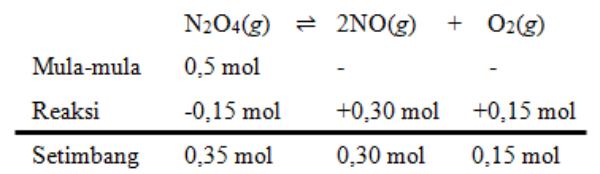
- Tentukan konsentrasi zat-zat saat setimbang
M =Vn
[N2O4]=Vn N2O4 saat setimbang=2 L0,35 mol=0,175 M=1,75×10−1 M
[NO]=Vn NO saat setimbang=2 L0,30 mol=0,15 M=1,5×10−1 M
[O2]=Vn O2 saat setimbang=2 L0,15 mol=0,075 M=7,5×10−2 M
- Hitung tetapan kesetimbangan
Kc=[N2O4][NO]2[O2]
Kc=[1,75×10−1][1,5×10−1]2[7,5×10−2]
Kc=(1,75×10−1)(2,25×10−2)(7,5×10−2)
Kc=1,75×10−116,875×10−4
Kc=9,64× 10−3
Jadi Kc untuk soal di atas adalah 9,64 x 10-3.