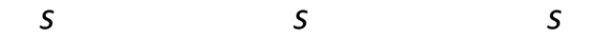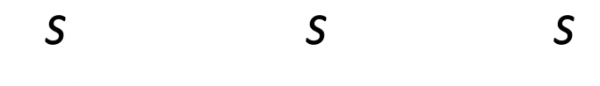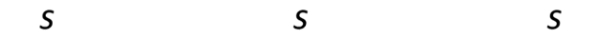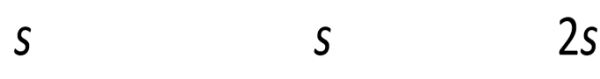Kelarutan adalah jumlah maksimum zat yang dapat dilarutkan dalam sejumlah pelarut. Kelarutan dapat dinyatakan dalam dua jenis.
- Untuk zat yang mudah larut: dinyatakan dalam gram/100 gram air.
- Untuk zat yang sukar larut: dinyatakan dalam mol/L atau kemolaran.
Kelarutan padatan A dalam dua pelarut:
Pelarut air (50 mL) : dapat melarutkan 25 g padatan A
Pelarut eter (50 mL) : dapat melarutkan 5 g padatan A
Berdasarkan hal ini dapat diketahui bahwa kelarutan padatan A lebih tinggi dalam pelarut air (pelarut polar) dibandingkan dalam pelarut eter (pelarut nonpolar). Senyawa yang dapat larut lebih baik dalam pelarut polar termasuk jenis senyawa polar.
Diketahui:
Vair=Veter=50 mL
ρair=1 mlg
ρeter=0,713 mlg
mA dalam air=25 g
mA dalam eter=5 g
Mr A=50 g.mol−1
Ditanya: s untuk pelarut air dan eter dalam g/100 g air dan dalam mol/L?
Dijawab:
mair=ρair×Vair
=1 mLg×50 mL
=50 g
meter=ρeter×Veter
=0,713 mLg×50 mL
=35,65 g
Menyatakan kelarutan padatan A dalam air
mol A=MrmA dalam air
=50 gmol−125 g
=0,5 mol
Cara pertama : dinyatakan dalam mol/L atau kemolaran
sA=Vairmol A
=0,05 L0,5 mol
=10 Lmol
Cara kedua : dinyatakan dalam gram/100 gram air
sA=mairmA dalam air=50 g air25 g=100 g air50 g
Menyatakan kelarutan padatan A dalam eter
mol A=MrmA dalam eter
=50 gmol−15 g
=0,1 mol
Cara pertama : dinyatakan dalam mol/L atau kemolaran
sA=Vetermol A
=0,05 L0,1 mol
=2 Lmol
Cara kedua : dinyatakan dalam gram/100 gram air
sA=metermA dalam eter=35,65 g eter5 g=100 g eter14,03 g
Pelarut paling sesuai untuk padatan A adalah pelarut air karena A termasuk senyawa polar dengan kelarutan 10 mol/L atau 50 g/100 g air.