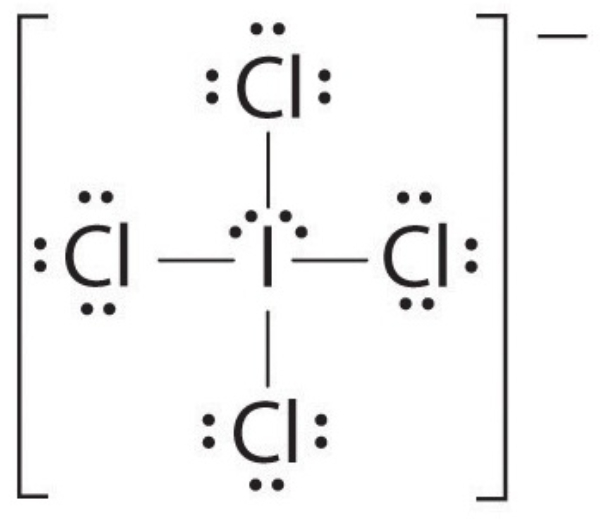Ikatan ion adalah ikatan yang terjadi akibat perpindahan elektron dari satu atom ke atom lain (serah terima elektron). Ikatan ion terbentuk antara atom yang melepaskan elektron (logam) dengan atom yang menangkap elektron (nonlogam). Atom logam setelah melepaskan elektron berubah menjadi ion positif. Sedangkan atom nonlogam setelah menerima elektron berubah menjadi ion negatif. Antara ion-ion yang berlawanan muatan ini terjadi tarik-menarik (gaya elektrostastis) yang disebut ikatan ion (ikatan elektrovalen).
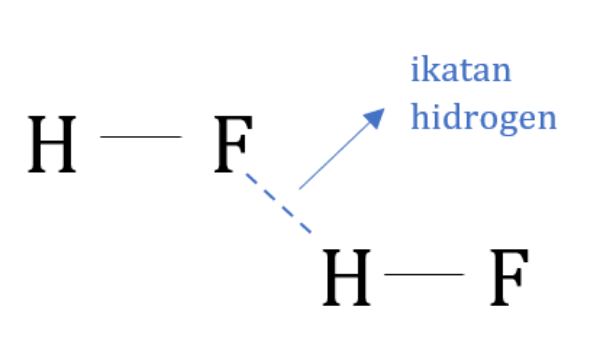
Ikatan kovalen adalah ikatan yang terjadi akibat pemakaian elektron bersama. Umumnya, ikatan kovalen terjadi antara atom-atom nonlogam.
Konfigurasi elektron dan jenis ikatan yang dimiliki oleh senyawa-senyawa dalam pilihan jawaban adalah sebagai berikut.
19K = 2, 8, 8, 1 → elektron valensi 1 → Golongan IA (logam) → agar stabil melepas 1e-
17Cl = 2, 8, 7 → elektron valensi 7 → Golongan VIIA (nonlogam) → agar stabil menarik 1e-
Reaksi: K+ + Cl- → KCl
19K = 2, 8, 8, 1 → elektron valensi 1 → Golongan IA (logam) → agar stabil melepas 1e-
8O = 2, 6 → elektron valensi 6 → Golongan VIA → (nonlogam) → agar stabil menarik 2e-
Reaksi: 2K+ + O2- → K2O
1H = 1 → elektron valensi 1 → Golongan IA (nonlogam) → agar stabil memerlukan 1e-
8O = 2, 6 → elektron valensi 6 → Golongan VIA (nonlogam) → agar stabil memerlukan 2e-
Terbentuk 2 ikatan kovalen tunggal H−O−H
6C = 2, 4 → elektron valensi 4 → Golongan IVA (nonlogam) → agar stabil memerlukan 4e-
8O = 2, 6 → elektron valensi 6 → Golongan VIA (nonlogam) → agar stabil memerlukan 2e-
Terbentuk 2 ikatan kovalen rangkap O=C=O
1H = 1 → elektron valensi 1 → Golongan IA (nonlogam) → agar stabil memerlukan 1e-
17Cl = 2, 8, 7 → elektron valensi 7 → Golongan VIIA (nonlogam) → agar stabil memerlukan 1e-
Terbentuk 1 ikatan kovalen tunggal H−Cl
12Mg = 2, 8, 2 → elektron valensi 2 → Golongan IIA (logam) → agar stabil melepas 2e-
8O = 2, 6 → elektron valensi 6 → Golongan VIA (nonlogam) → agar stabil menarik 2e-
Reaksi: Mg2+ + O2- → MgO
20Ca = 2, 8, 8, 2 → elektron valensi 2 → Golongan IIA (logam) → agar stabil melepas 2e-
17Cl = 2, 8, 7 → elektron valensi 7 → Golongan VIIA (nonlogam) → agar stabil menarik 1e-
Reaksi: Ca2+ + 2Cl- → CaCl2
4Ba = 2, 2 → elektron valensi 2 → Golongan IIA (logam) → agar stabil melepas 2e-
17Cl = 2, 8, 7 → elektron valensi 7 → Golongan VIIA (nonlogam) → agar stabil menarik 1e-
Reaksi: Ba2+ + 2Cl- → BaCl2
Jadi kelompok senyawa yang mempunyai ikatan ion adalah MgO, CaCl2, dan BaCl2.